华福波1,张伟1,薛正良2, 龚树山3, 张文海3
( 1.武汉科技大学钢铁冶金与资源利用省部共建教育部重点实验室,湖北 武汉430081 ;
2.武汉科技大学钢铁冶金新工艺湖北省重点实验室,湖北 武汉430081 ;
3.北京闪铁科技有限公司,北京100083)
摘 要:高炉冶炼过程中铁水最终渗碳量接近饱和,相比而言,闪速炉中没有固体炉料的压迫作用,无法发生像高炉炉缸内死料柱根部与铁水之间的渗碳反应,最终渗碳量难以预料。以还原铁粉和化学纯石墨为原料,利用管式电阻炉升温到1855K熔化铁粉,以高纯 N2 作为保护气体研究焦炭在铁水中溶解的动力学,为闪速炼铁工业化打下基础。实验结果表明,在自然对流条件下,不考虑溶解速率系数kt随溶解时间的变化时,得到了各组实验条件下确定的kt值分别为4.20 μ m / s (第1组)、 5.28 μ m / s (第2组)和6.50 μ m / s (第3组);考虑溶解速率系数随溶解时间变化时,焦炭的kt\值随着溶解时间的增加而降低,且仅受传质控制;当铁碳熔体中有硫存在时,溶解速率随着铁浴中硫含量的增加而降低。
关键词:非高炉炼铁;熔融还原;闪速炼铁;渗碳;溶解速率
高炉炼铁工艺的发展由于流程长、对贫杂资源适应性差而受到严重制约,尤其是焦化、烧结、球团等原料制备工艺中产生的环境问题日益突出。因此,以非结焦煤为能源的非高炉炼铁技术[1-2]成为钢铁界的研究热点。经过长时间的研究与发展,目前形成了以直接还原[3-7]和熔融还原[ 8-15]为主体的现代化非高炉炼铁技术体系。闪速炼铁工艺[16-18]是近年来提出的一种新兴熔融还原炼铁技术。考虑到气固渗碳非常有限,闪速炼铁新工艺中铁水渗碳环节中碳的迁移主要发生在铁水穿行焦炭床时的固液渗碳过程。闪速炼铁工艺中铁水适宜的碳的质量分数应为3.0%~4.0%之间,此时的铁水既可以满足较低的凝固点,避免运输过程中因铁水降温而发生铁水包或鱼雷罐冻结事故,也可以减少转炉炼钢工序中为了脱碳而增加的吹氧量[19]。因此,有必要设计高温实验对焦炭在铁水中溶解的动力学进行研究,分析焦炭在铁液中的溶解机理,为闪速炼铁工业化提供理论基础。
Mourao等设计了一组实验研究铁碳熔体中的碳素溶解机理[20-21],在1623~1875K温度范围内研究了碳质材料在铁碳熔体中的溶解速率。在感应炉中熔化纯电解铁和石墨粉的混合物,连续通入流量为7.17×10-6m3/s的氩气对炉体进行保护。碳样品用氧化铝棒夹持预热后浸入熔体,样品浸渍一定时间后,从熔体中取出并冷却。通过样品的失重量来确定熔体中碳的溶解量。该实验方法的优点为不受铁水中碳浓度偏析的影响,保证了实验结果的可靠性。但由于溶解后的碳样品表面会沾有一层铁液,所以为了得到准确的碳样品失重量,必须对溶解后的碳样品进行铁分析,计算出溶解后的碳样品的铁含量。而且溶解后的碳样品表面不规整,含铁分析也会有一定的难度。这些因素导致实验周期长、过程繁琐而不易进行。因此,本次实验进行了相应的改进。直接取样分析C 、 S含量,进而计算溶解速率系数,增加了实验结果的可操作性。
1 焦炭在铁水中的溶解实验
1.1 实验材料及设备
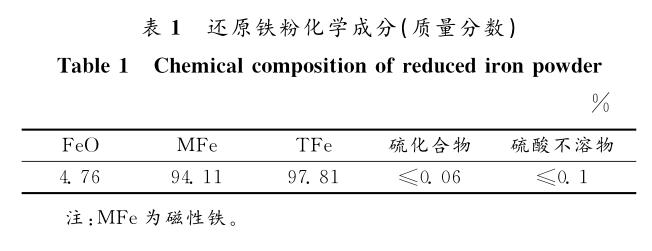
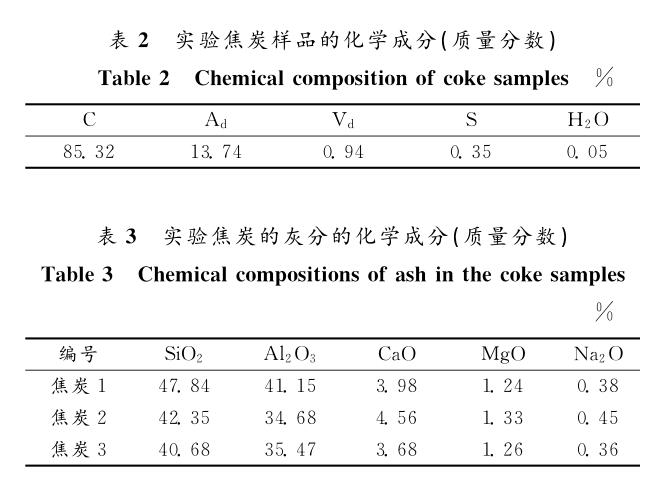
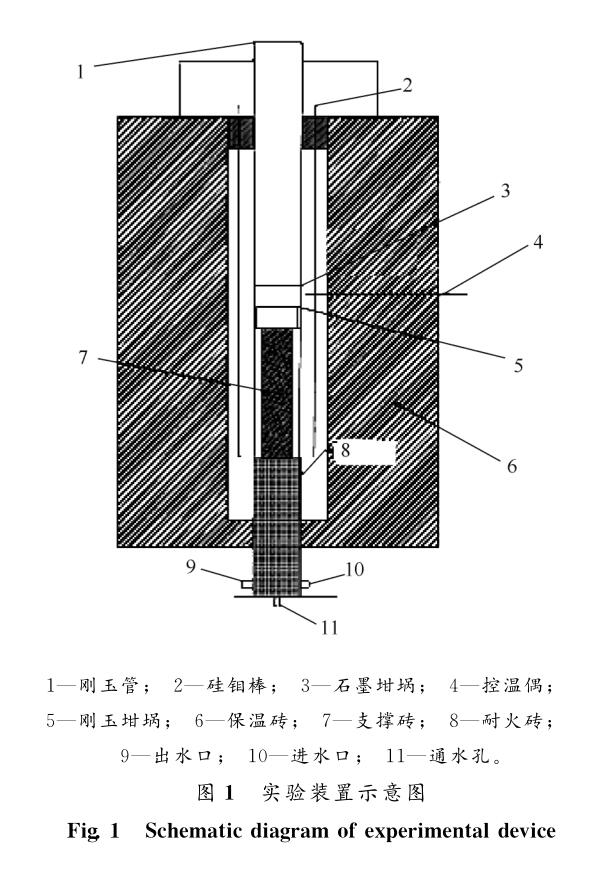
实验采用还原铁粉作为渗碳原料,其化学成分如表1所示。实验使用上海实验电炉厂制造的管式电阻炉,炉内安装有内径100mm 、长度1 200mm 的刚玉管。外径和内径分别为82 、 74mm 的刚玉坩埚,外径和内径分别为96 、 83mm 的石墨坩埚,向还原铁粉中配加一定量的化学纯石墨(质量分数为98.0% )作为原始碳含量。通过研磨同批的大块焦炭获得边长为20mm 左右的立方体焦炭,其化学成分及其灰分的化学成分分别见表2和表3 。以纯度为99.999%的高纯氮气作为保护气体,用内径为3mm的石英管抽取铁样。用 C - S分析仪分析铁样的碳含量和硫含量,用 SEM 检测部分溶解的焦炭样品表面结构。本研究所用实验装置如图1所示。
由表1可知,实验所用还原铁粉中含有少量的FeO ,为了去除其对实验结果的影响,在还原铁粉中配加一定量的化学纯石墨可提前将 FeO 还原成Fe 。根据直接还原机理可计算出完全还原 FeO 所需的石墨量。计算过程如下:
mFeO=4.76%mz (1)
FeO+C=Fe+CO (2)
mC = nCMC = nFeO MC (3)
式中:mFeO 为还原铁粉中的FeO的质量;mz为还原铁粉的质量;mC为还原FeO 所需的碳量;nC为碳的物质的量;MC为碳的摩尔质量;nFeO为FeO的物质的量。解得mC =3.17g 。由于化学纯石墨的纯度为 98.0% ,所以 实际添 加 量 应 为 3.17/ 0.98=3.23g 。也就是至少要向还原铁粉中添加3.23g 的化学纯石墨,才能完全将铁粉中的 FeO 还原成 Fe ,去除 FeO 对实验结果的影响,保证实验结果的可靠性。
1.2 实验过程
等温实验中的控温温度为1873K ,通过测温热电偶的实测值可知,炉内恒温带的温度为1855K ,且恒温带宽度能够确保样品位置处于恒温区域。
将装有400g 还原铁粉和一定比例化学纯石墨混合物的刚玉坩埚放进石墨坩埚后,用细绳将石墨坩埚缓慢放入刚玉管中。按5L / min的流量向刚玉管内通入氩气,封住刚玉管两端以检查气密性,保证保护气体全部从刚玉管中流出。通气10min后,改流量为2L / min 。在炉子底部通冷却水,以保护密封圈能正常工作。
当控温温度达到1873K后,恒温300min ,以保证在恒温条件下取样。当温度达到1873K 并恒温2h后,将干燥焦炭样品用耐火钳夹持放入刚玉坩埚中,并开始计时。
开始计时后,按2、4、6、8、10、15、20、25、30、35、40、50、60、80 、100、120min的时间节点取样。将石英管从炉顶插入刚玉管中的刚玉坩埚,轻微搅动后抽取铁液,使取得的铁样对该时的铁液成分具有较好的代表性。抽取成功后迅速取出并放入水中进行淬火,而后敲碎石英管取出铁样,待冷却后装入样品袋并按取样时间顺序编号。
每组实验抽取16个铁样,按实际抽取的铁样来看,每次成功抽取的铁样的长度都在30mm 左右。但是随着取样的不断进行,坩埚中的铁液会逐渐减少。为了探究坩埚中铁液的不断减少是否会影响后期的实验结果,特做了以下计算:
V = S1L (4)
S1=πR21 (5)
Vt =15V (6)
mt = ρVz (7)
对刚玉坩埚:
S2=πR22 (8)
则取 样 完 成 后,坩 埚 中 铁 液 液 面 下 降 高 度Δ h 为:

式中:V为每次取样的平均体积;L为每次取样的平均长度;S1 为石英管截面积;R 1 为石英管内径;Vt为整个实验取样的总体积;mt 为实验所取铁样总质量;S2为刚玉坩埚截面积;Vz为实验所取铁样总体积;ρ为铁液密度;R2为刚玉坩埚内径; Δh为取样前后铁液液面降低的高度。代入相关数据计算得Δh=0.74mm ,而取样前铁液深度为13.04mm 。由此可知,刚玉坩埚中的铁液量满足取样要求,不会对实验结果产生重大影响。
将取得 的 铁 样 依 次 放 到 天 平 中 称 取 0.42~0.43g ,将铁样贴上标签后送到 C -S 分析 室进行分析。
2 动力学理论
本文研究的重点是焦炭与铁液熔体的相互作用(焦炭的溶解)。当焦炭与液态铁接触时,碳的溶解通过以下2个基本步骤 [22 -24] 完成:第1步是发生碳原子解离固体结构成为溶解碳的界面反应;第 2 步是溶解碳通过焦炭固体附近液体边界层向铁液熔体的质量传递。液态铁碳熔体中焦炭溶解的质量流率j可定义为:
j = kt(Cs-Cb) (10)
式中: Cs 和 Cb分别为饱和碳含量和瞬时碳含量;kt为总溶解速率系数,并由式(11)计算得出。

式中: km 为碳在固体碳和弥散液体之间的传质系数;kb为界面反应系数。km、kb 分别为铁浴物理条件和化学活性对整个溶解过程的作用[20]。由 式(11)可知 kt值取决于参数kb和km的大小,如果kb远大于km,则系数由液体边界层的传质控制,反之亦然。如果kb和km的值成比例也会影响系数。kt值已被若干研究者通过改变影响固体样品周围液体流体动力学的实验条件(反之,影响km)所确定。当雷诺数小于一定值时固体附近液体边界层的传质可以控制溶解速率,而高雷诺数范围下时过程可能由界面反应控制[20- 21]。本研究是在1855K 恒温条件下进行,且坩埚中铁液没有大的波动,所以雷诺数较小,焦炭溶解速率受固体附近液体边界层的传质控制。
焦炭在铁液中的溶解速率可通过测量铁液中的碳含量来确定。溶解碳的总质量Wcd,通过最后一次取出的铁样的碳含量与还原铁粉质量相乘求出。式(12)用于计算溶解总速率系数:

式中:t为样品的总浸渍时间;As为样品浸入部分的表观表面积。 As可通过以下方程计算:

式中:V1 为样品浸入部分的体积;g 为重力加速度;m1 为样品质量;S3为样品的底面积;H 为样品浸入深度;a为样品边长。
由式(12 )可知,溶解速率系数与浸渍时间、 Cb和 Wcd有关。为了确定部分溶解的焦炭样品的表面形状与成分,以及铁浴中的硫含量对渗碳行为中碳的迁移规律的影响,对实验结果的介绍和讨论如下。
3 结果与讨论
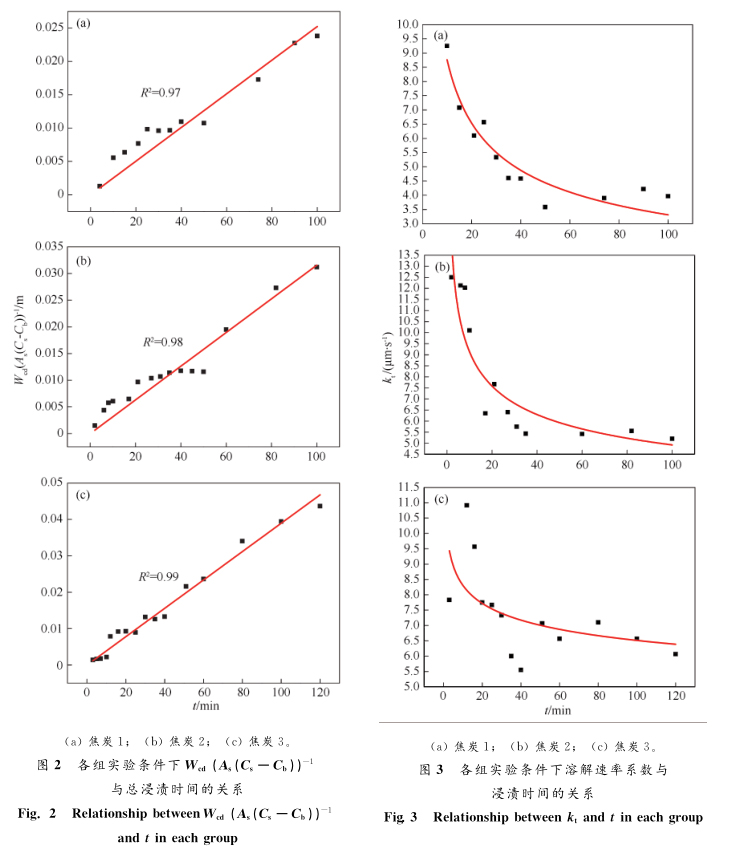
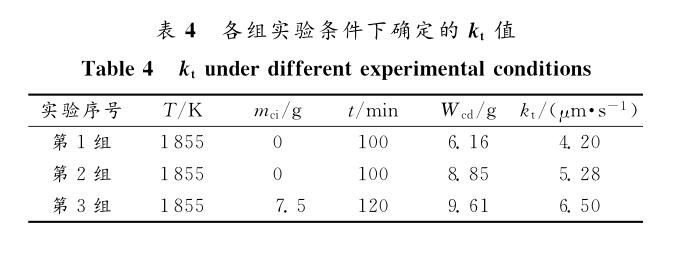
由式(12)可知,Wcd (As(Cs-Cb))-1与t呈正相关关系,因此对实验数据进行线性回归分析可得到kt值,如图 2 所示。本研究确定kt值在3.58和12.5μ m/ s之间(1855K ),实验确定kt的一些典型值见表 4 。由表 2 和表 3 可知,由于实验焦炭样品的灰分成分有差异,因此焦炭在铁液中溶解时表面形成的渣相有差异,使得kt 有差异。同时kt是碳含量和样品浸渍时间的函数,根据动力学分析可知,影响流体动力学条件的铁浴密度取决于碳含量和温度,且本实验是在1855K 恒温条件下进行的,所以本研究中原始碳含量 mci是影响流体动力学条件的唯一操作变量,且kt值也将受到铁浴化学活性的影响。
3.2 溶解速率随时间变化
3.2.1 浸渍时间对溶解速率的影响
通过对连续浸渍焦炭样品进行实验,研究黏性层的形成和熔融铁渗入样品孔隙对溶解速率的影响。将焦炭投入铁液后,每次取得的铁样都会对应一个碳含量并以此估计焦炭的溶解速率系数kt。由图3可知,连续浸没实验确定的kt值随着浸渍时间t的增加而单调减小,这是由于样品的灰分含量和多孔结构在溶解过程中的作用造成的。
通过SEM 检查几个焦炭样品溶解后的表面结构,并分析样品表面的化学组成,几张典型的显微照片如图 4 所示。从图 4 中可以看出,焦炭样品的大部分孔隙都被液态金属所填充。表5中给出了部分溶解的焦炭样品渣状层的化学分析。由表5可以看出,部分溶解的焦炭样品渣层主要含有金属铁和铝。假设除铁以外的所有元素以炉渣的形式存在,则将化学组成转化为氧化物。炉渣层中Al2O3的质量分数为70%~80% ,SiO2的质量分数为9%~18% ,CaO 的 质 量 分 数 为0.8% ~4% 并 含有微量的TiO2、 K2O和P2O5 。因此,渣状黏性层阻碍了溶解过程。由表2和表3可知,这是由于随着溶解的进行,样品表面上的灰分含量逐渐增加而形成厚的黏性层,减少了可用于溶解的有效表面积。此外,在溶解开始时渗透到样品孔隙中的液态金属可能被吸附在孔隙内而达到碳饱和,从而限制焦炭中的碳溶解到铁碳熔体中。

3.2.2 硫对溶解速率的影响
虽然前面提到溶解速率不是由相界面反应控制,但是硫等表面活性元素可能会阻碍相界面反应。因此,存在硫等表面活性元素时的kb值将减小。
图5为焦炭样品在铁碳熔体中溶解后,熔池硫含量对焦炭样品kt的影响。由图 5 可知焦炭样品的kt值随着铁浴中硫含量的增加而降低。这是因为一方面硫在铁液中以FeS 状态存在,抑制了Fe3C的生成,使铁水碳含量降低。另一方面,焦炭硫含量较大时,焦炭表面对硫有吸附作用,使焦炭与铁液接触面积减少,阻碍了固体碳向铁碳熔体中的扩散,使焦炭溶解速率减小。
4 结论
(1)在自然对流下溶解速率系数的值仅受固体附近液体边界层的传质控制,相界面反应的贡献可忽略不计。
(2)不考虑溶解速率系数kt 随溶解时间的变化时,得到了各组实验条件下确定的焦炭的kt值分别为4.20μ m/s(第1组)、5.28μm/s(第2组)和6.50μ m/s(第3组)。考虑溶解速率系数随溶解时间的变化时,焦炭的kt值在3.58~12.5μm/s之间,且随着溶解时间的增加而降低。
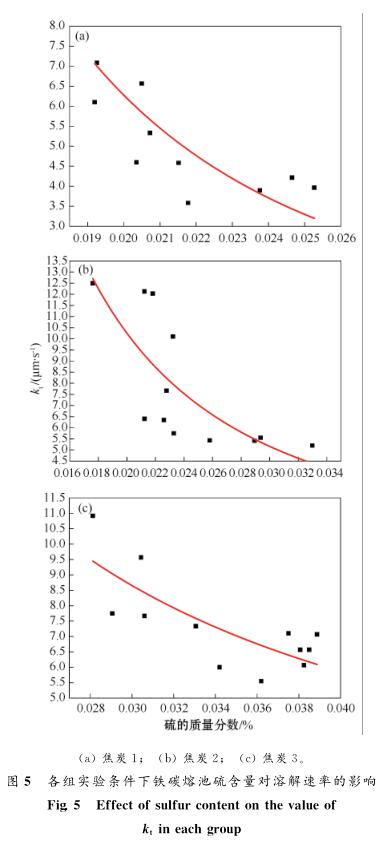
(3)溶解速率系数还受铁碳熔体中硫含量的影响。当铁碳熔体中硫的质量分数从0.0170%增大到0.0330%时,焦炭的 kt 值从12.5μm/s降低到5.20μ m /s,说明溶解速率随着铁浴中硫含量的增加而降低。
